Ha mort un home presumptament apunyalat en plena llum del dia a Platja d’en Bossa
El succés ha ocorregut poc després de les 16.30 hores i el suposat agressor hauria fugit del lloc dels fets




L'assaig durarà diversos mesos i anirà seguit de la fase 3. Si els resultats fossin positius, una vegada avaluats per les autoritats reguladores competents, s'autoritzaria la comercialització en territori europeu, ha explicat avui el ministre de Sanitat, Salvador Illa
 182
182
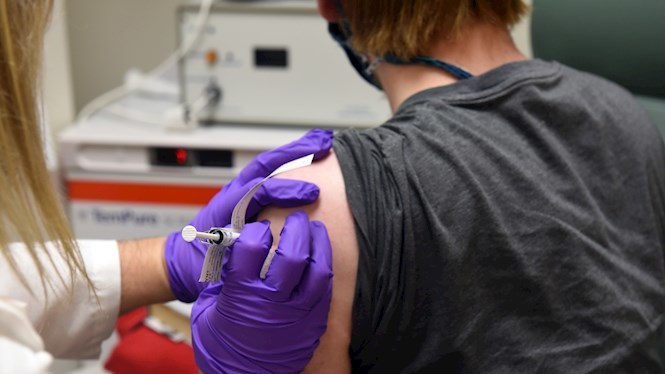
L’Agència Espanyola de Medicaments i Productes Sanitaris (Aemps) del Ministeri de Sanitat ha autoritzat aquest divendres el primer assaig clínic al nostre país per una vacuna anticovid, que serà en fase 2, és a dir, en humans.
Ho ha anunciat el ministre de Sanitat, Salvador Illa, en roda de premsa en la qual ha agregat que la vacuna està desenvolupada per l’empresa Janssen i que a l’assaig a Espanya participaran 190 voluntaris. També hi participaran altres dos països Europeus, Bèlgica i Alemanya. L’assaig en fase 1 s’ha fet als Estats Units i Bèlgica.
En total participaran 550 voluntaris sans dels tres països europeus per avaluar el rang de dosi i diferents pautes d’administració. La recerca es realitzarà en adults i inclou dos grups de voluntaris, un de 18 a 55 anys i un altre de 65 i més. El reclutament començarà “de manera immediata”. Els assajos clínics es duran a terme als Hospitals La Paz i La Princesa de Madrid i a l’Hospital Marquès de Valdecilla de Santander.
L’assaig clínic durarà diversos mesos i anirà seguit d’un en fase 3, l’última abans de tenir una autorització del producte. “I anirem veient les pròximes setmanes i mesos com evoluciona això”, ha assenyalat el titular de Sanitat.
Aquesta vacuna, denominada Ad26.COV2.S, usa una tecnologia basada en un adenovirus recombinant no replicatiu per generar una resposta immunològica enfront d’una de les proteïnes del coronavirus. Els assajos són imprescindibles per garantir la qualitat, seguretat i eficàcia de les vacunes.
Si els resultats fossin positius, una vegada avaluats per les autoritats reguladores competents, s’autoritzaria la comercialització en territori europeu, ha dit Illa.
L’Agència Espanyola de Medicaments i Productes Sanitaris manté contacte amb diferents companyies per dur a terme més assajos clínics d’aquest tipus a Espanya-
Disculpau, els comentaris es troben tancats
El succés ha ocorregut poc després de les 16.30 hores i el suposat agressor hauria fugit del lloc dels fets

El col·lectiu d'infermeres defensa les competències de les professionals en tasques de gestió

Demanen solidaritat entre els vaixells fondejats perquè deixin gaudir d'aquest fenòmen als qui l'observen des de terra
